CAR-T细胞治疗多发性骨髓瘤(MM)目前呈现指的期待的效果,但通常有严重的毒性。CAR-NK细胞在重新定向对抗耐药骨髓瘤细胞时可能发挥更小的毒性。
NKG2D通过靶向多达8种应激配体(NKG2DL)来识别并杀死受感染的细胞和癌细胞,即MICA、MICB和ULBP,这些配体在病毒感染、DNA损伤或转化的细胞上过表达,通常在健康组织中不表达。超过70%的人类癌症会上调NKG2D配体的表达。

文中NKAE为实验室大量活化和扩增的自体NK细胞,临床效果良好,无毒性反应。还比较了CAR-NKAE细胞与记忆性CAR-T细胞的体外疗效。
作者首先使用慢病毒转染的方式生产CAR,慢病毒载体(NKG2D-CAR:LV)在293 T细胞中通过连续稀释转导滴定,通过流式细胞术分析MM细胞中的NKG2D配体表达。随后从样本中分离PBMC进行NK和T细胞的分选。两种细胞类型NKG2D阳性细胞的百分比高于未转导细胞,中位荧光强度(MFI)增加。6天后,表达CAR的NKAE细胞的表达保持稳定,T细胞的转导更稳定。

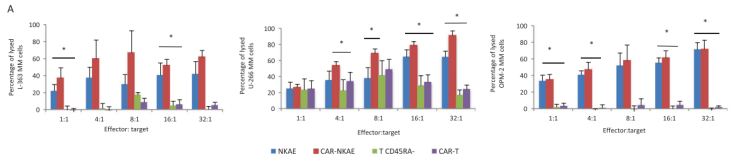
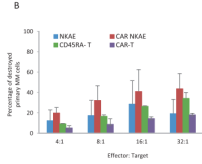
采用EuTDA法(PerkinElmer,AD0116)评估细胞毒性。NKG2D-CAR-NKAE细胞可根除MM细胞。以U-266、L-363、OPM-2骨髓瘤细胞和原代MM浆细胞作为靶细胞,与效应细胞按指定的靶细胞(E:T)比例孵育4小时。为检测CAR转导的效应细胞的安全性,以供体PBMC、CCD-18Co和NL-20细胞系为靶点,进行细胞毒性试验。NKAE细胞对U-266 MM细胞系表现出强大的细胞毒性活性,在最大E:T比值(32:1)时,破坏了77.7%的MM细胞。与未转导的NKAE细胞相比,CAR-NKAE细胞表现出更好的细胞毒性,在较低的E:T比值(8:1)下破坏了100%的MM细胞。与未转导的NKAE细胞、记忆T细胞和CAR-T细胞相比,CARNKAE细胞对MM细胞系表现出更强的细胞毒性。
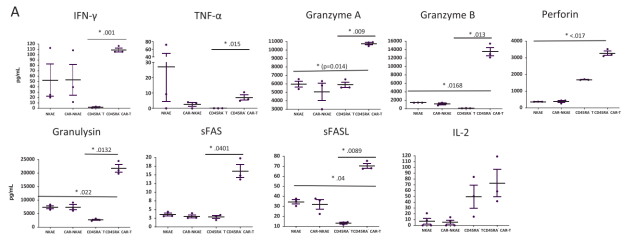
作者使用流式细胞术检测细胞因子释放,效应细胞和靶细胞以16:1的比例孵育4小时。NKAE细胞和T细胞分泌了所有所分析的细胞因子。T细胞的细胞毒性机制普遍上调,细胞因子、溶解颗粒和可溶性Fas/FasL的释放增加。与NK细胞相比,细胞凋亡配体在NKAE细胞和CAR-NKAE中TRAIL表达增加,FasL表达减少。
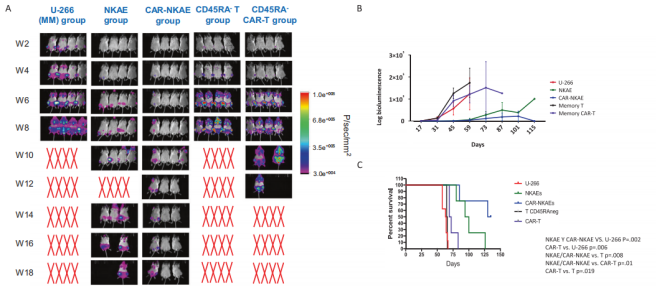
除此之外,NKG2D-CAR-NKAE细胞在体内显示出强大的疗效。接受NKAE细胞和CAR-NKAE细胞的小鼠存活时间是对照组(MM组)小鼠的两倍。接受记忆T细胞或CAR-T细胞的小鼠存活时间与未处理组相同,CAR-T细胞的小鼠只存活了20天。
NKG2D-CAR转导在体外增强了强大的抗肿瘤活性。虽然记忆T细胞也易受CAR转导的影响,但它们在自体环境中对MM无效。相比之下,自体CAR-NKAE细胞显示出强大的细胞毒性活性,没有毒性,并且在小鼠模型中完全消除了MM的生长。本研究使用携带NKG2D-CAR的自体NKAE细胞治疗,为多发性骨髓瘤治疗提供了重现性和可行性。
文章来源:Blood Cancer Journal (2021) 11:146 ;
https://doi.org/10.1038/s41408-021-00537-w
DELFIA® EuTDA法综合评价
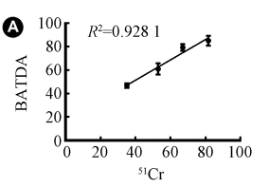
中检院曾发文题为《免疫细胞治疗制剂体外杀伤效力评价》,文中对51Cr 、BATDA 、CAM 、CytoTox-Glo 、PKH、EliSpot和LDH法进行了杀伤效果评价。其中51Cr同位素法是检测杀伤的金标准,结果总结,BATDA法与51Cr 释放法的平行性最好,作用时间明显缩短,可重复性高,对悬浮靶细胞和贴壁型靶细胞均具有很好的适用性。可重复性好,可以满足免疫细胞体外杀伤效力检测的需要。
来源于优宁维药物研发官网

