T淋巴细胞(T细胞)是适应性免疫系统的主要细胞组成部分,负责介导基于细胞的免疫反应,以保持宿主的健康和预防各种类型的疾病。T细胞是由胸腺中骨髓(BM)来源的胸腺祖细胞分化而来,可分为γδ T细胞和自然杀伤T(NKT)细胞外,还可分为CD4+和CD8+αβ T细胞。αβ T细胞识别由抗原呈递细胞(APCs)上的MHC分子呈递的抗原。在识别同源抗原T细胞受体(TCR)和共刺激分子和细胞因子,激活CD4+CD8+T细胞,扩增和分化来杀死感染细胞,产生细胞因子和调节免疫反应。一些T细胞发育成记忆T细胞,在重新遇到相同的抗原时可表现出快速的效应功能,并为宿主提供强有力的和长期的保护。与此同时,也存在一个CD4+T细胞亚群,称为调节性T(Treg)细胞,它们维持外周免疫耐受。在过去的几十年里,我们对T细胞的分类、分化、细胞和分子调控机制,特别是在健康条件和免疫相关疾病中的表型和功能的了解有了显著的进展。
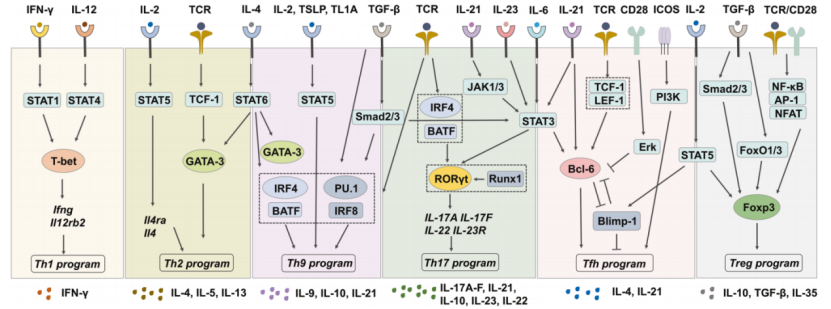
图1:CD4+ T辅助细胞分化示意图
From:T cells in health and disease,Signal Transduction and Targeted Therapy (2023) 8:235,Lina Sun,et.
CD4+ T辅助细胞(Th)是一组异质性的T细胞,在免疫反应中起着核心作用。CD4+ T细胞可以激活肽-MHCII类复杂的APCs,共刺激和细胞因子信号和分化,细胞因子和关键的TFs,如Th1,Th2,Treg,Tfh,Th17,Th9,Th22,CTLs等。
Th1细胞是通过产生促炎细胞因子IFN-γ来保护宿主免受细胞内细菌和病毒感染。IL-12和IFN-γ是Th1分化所必需的两种细胞因子。TCR刺激和IFN-γ-STAT1信号诱导T-bet的表达,主要TF驱动Th1分化,抑制Th1/Th17谱系。T-bet可以直接与Ifng基因结合,增加IFN-γ的表达,同时促进IL-12Rβ2的表达。IL-12信号通过激活STAT4,反过来,维持T-bet的表达。这些都有助于Th1分化。
Th2细胞由TF GATA-3表达和细胞因子IL- 4、IL-5和IL-13的分泌而分化,可以保护宿主免受蠕虫感染,促进组织修复,并促进慢性炎症,如哮喘和过敏。由树突状细胞(DCs)和先天淋巴样细胞ILC2分泌的IL-4与CD4+T细胞上的IL-4R结合,通过STAT6磷酸化促进GATA-3的表达,并随后产生Th2相关的IL4,IL5,IL13细胞因子。激活的CD4+T细胞自分泌IL-4进一步促进Th2分化。此外,GATA-3通过抑制Th1相关基因,如Tbx21、IFNγ、STAT4和IL-12Rβ2,来抑制Th1细胞分化。由IL-2启动的STAT5信号通路是维持IL4RA的表达和增加IL4染色质所必需。其他TFs如NFAT1、c-Maf、IRF4和JunB可以通过诱导IL-4的产生来促进Th2分化。此外,被TCR刺激激活的TCF-1,促进GATA-3的表达来启动Th2细胞的分化
Th9细胞在感染性疾病、过敏、癌症和自身免疫免疫中发挥关键作用。Th9细胞可以在IL-4和TGF-β存在下被TCR刺激诱导,IRF4和PU.1显著增加,除了IL-9,IL-10和IL-21也由Th9细胞产生。IL-4信号通路介导的STAT6磷酸化诱导GATA-3、IRF4和BATF的表达,促进IL-9转录和Th9细胞分化。此外,TGF-β信号通路激活SMADs(SMAD2/3)、PU.1和IRF8,促进Th9细胞分化。此外,IRF4,PU.1、IRF8和BATF形成一个TF复合物,与IL9位点结合并调节Th9分化。此外,IL-2、TSLP和TL1A诱导的STAT5磷酸化也促进了Th9细胞的分化。Th9细胞的分化也受到共刺激信号通路(CD28、OX40、GITR、Notch、和DR3)和其他细胞因子IL-1、IL-25、IL-7和IL-21。
Th17细胞以特征的细胞因子IL-17A-F、IL-21、IL-10、IL-23和IL-22的表达为特征,以及类固醇受体型核受体RORγt,有助于保护细胞外病原体,特别是在黏膜组织,以及慢性炎症和自身免疫性疾病。IL-6和TGF-β促进Th17细胞分化,而IL-21和IL-23稳定Th17。IL-6通过磷酸化STAT3促进RORγt的表达,而抑制TGF-β诱导的FOXP3的表达。RORγt通过直接靶向IL-17A、IL-17F、IL-17F、IL-22和IL-23R的表达。通过SMAD2/3传递的TGF-β信号可以维持STAT3的激活状态。自分泌IL-21通过激酶JAK1/3的激活激活STAT3,从而进一步增加IL-23R的表达。IL-23可促进STAT3的激活以稳定Th17的分化。最近的研究表明,Th17细胞具有很大程度的可塑性,这取决于TGF-β。TGF-β和IL-6诱导“经典”Th17细胞产生IL-17,IL-21,和IL-10,而IL-6,IL-1β,IL-23诱导“致病性”Th17细胞产生高水平的IFN-γ,GM-CSF,IL-22。TCR信号诱导促进IRF4和BATF(除RORγt)有助于Th17相关因子,如IL17、IL21、IL23R。Runx1通过诱导RORγt和直接相互作用促进Th17的发育,其他TFs,包括RORα、c-Maf、p65、NFAT和c-Rel,也参与了Th17的分化。
Tfh细胞是一种特殊的CD4+Th细胞,通过促进B细胞的增殖和成熟、GC反应和产生抗体来支持体液免疫应答。Tfh细胞表面PD-1和CXCR5高表达,共刺激受体CD40,CD40LG和ICOS,细胞因子IL-4,IL-21的分泌,STAT3和Bcl-6 Tfh核心作用在调节抗体反应。Tfh细胞的分化主要源于Bcl-6的作用,通过抑制Th1、T-bet、GATA-3和RORγt的表达来抑制Th1、Th2和Th17细胞的分化。抑制B淋巴细胞诱导的Blimp-1,Tfh也需要由Bcl-6作用完成。TCF-1通过与LEF-1和其他TFs,如BATF、STAT1/3/4/5、FOXP1、KLF2、IRF4、ETS1、BACH2、ASCL2、TOX2和Bhlhe40也参与调节Tfh细胞的分化。此外,Tfh细胞分化受共刺激信号调控,CD28刺激激活ERK抑制Tfh细胞分化而ICOS激活PI3K促进和维持Tfh细胞。Tfh细胞的分化的细胞因子方面,IL-6和IL-21分别通过作用STAT3和诱导Bcl-6的表达来促进Tfh细胞的分化。然而,IL-2/STAT5信号通路通过诱导Blimp-1的表达来抑制Tfh的分化。
Treg细胞是一种特殊的CD4+T细胞亚群,通过抑制免疫反应来维持免疫耐受。Treg细胞的特点是高表达IL-2Rα(CD25),抑制细胞因子IL-10,TGF-β,IL-35和调控TF Foxp3。TGF-β 和IL-2可以通过调控Foxp3的表达促进Treg细胞的分化,并且Foxp3对Treg细胞的维持和功能至关重要,涉及转录和表观遗传等机制。TCR/CD28刺激通过诱导NF-κB、AP-1和NFAT与Foxp3增强子/启动子区域的结合来触发Foxp3的表达。此外,TGF-β通过诱导SMAD2和SMAD3磷酸化增强Foxp3表达,STAT5也增加Foxp3的表达。
1
HTRF®技术原理
HTRF®细胞因子采用夹心分析法检测,使用两种不同的特异性抗体,一种用Eu(供体)标记,另一种用d2(受体)标记。当标记的抗体与同一抗原结合时,供体用光源(激光或闪光灯)激发,触发向受体的荧光共振能量转移(FRET),进而在特定波长(665nm)发出荧光。这两种抗体与样本中存在的细胞因子结合,从而产生FRET。信号强度与细胞因子浓度成正比。
实验仅需在空板中加入16μl检测样本,随后加入4μl检测抗体,孵育2小时,即可使用酶标仪进行读数。
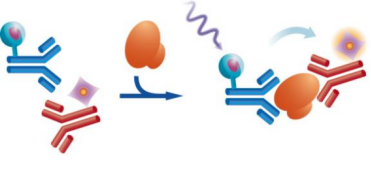
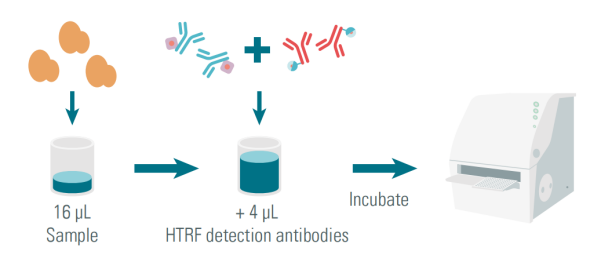
图2:HTRF技术原理及流程示意图
2
HTRF®技术优势
❖
均相体系,操作方便、无洗涤步骤、2h完成检测;
❖
节省样本,样本需求低至5μl;
❖
体系稳定,批次间重复性高;
❖
灵敏度高,实验窗口大,线性范围宽;
❖
高通量,兼容96/384/1536孔板。
来源于优宁维药物研发官网

