人血清白蛋白(HSA)在生物制药行业有着广泛的应用,包括血浆扩增、配方赋形剂、药物输送、伤口愈合以及作为融合搭档延长蛋白质药物的半衰期。由于人血清白蛋白的供应有限,无法满足临床需求,因此科研人员正在寻找其他来源的白蛋白,例如通过基因工程生产重组人血清白蛋白,以及各种各样的白蛋白融合蛋白已经被生产出来,以延长融合蛋白的循环半衰期,同时保持其活性。
目前,重组白蛋白的生产主要依赖于基因工程方法,通过酵母、CHO细胞或大肠杆菌等表达系统表达目标蛋白,再进行分离纯化等工艺。然而,在表达和纯化过程中,存在一些技术难题,如表达水平低、翻译后修饰不完全、纯化步骤繁琐且收率低等。
为了解决重组白蛋白融合蛋白纯化步骤繁琐且收率低的问题,Astrea Bioseparations与Albumedix【重组白蛋白产品的领先生产商和白蛋白融合蛋白技术的开发商(Veltis®)】合作开发了AlbuPure®,一种高度稳定、稳健、无毒、具有高结合能力、高回收率和高纯度的亲和色谱。符合ISO 9001质量标准的生产环境,可用于白蛋白及白蛋白融合蛋白的纯化和cGMP生产。
AlbuPure®是一种新型合成三嗪配基,源自Astrea Bioseparations的“Mimetic Ligand™ ”技术,并与其专利PuraBead®6HF琼脂糖基质偶联。该技术提供了稳定的基架和配体,可以使用1 M NaOH进行清洁,寿命较长。
AlbuPure® 性 能
|
Ligand: |
Synthetic triazine |
|
Adsorbent appearance: |
White |
|
Mean particle size: |
90±10um |
|
Base matrix: |
Highly cross-linked 6% near-monodisperse beaded agarose (PuraBead® 6HF) |
|
Binding capacity: |
>35 g/L* |
|
Operational flow rate: |
Up to 600 cm/hr |
|
Packing conditions: |
Saline solution at a constant pressure of 1.5 bar (~22 psi) |
|
Chemical stability: |
Stable in all commonly used buffers and solutions |
|
Sanitization: |
0.5 to 1.0 M NaOH, 25℃ |
|
Storage: |
2-30℃, 20% ethanol / 80% 0.1 M NaCl (v/v) |
|
*Performed using scFv albumin fusion fermentation supernatant loading to 10% breakthrough at 240 cm/hr, pH 4.5 |
|
AlbuPure®捕获和纯化重组白蛋白融合蛋白案例分享:
材料与方法
使用AlbuPure®在自动色谱工作站上纯化Albumedix酵母表达系统生产的不同白蛋白融合蛋白IL-1ra和anti-HIV gp41,在上样前都经过预处理。
未结合蛋白和结合不紧密的蛋白通过平衡缓冲液去除。结合的非靶标蛋白随后使用一系列增加pH的缓冲液洗脱。白蛋白融合蛋白使用含有辛酸钠的缓冲液选择性地洗脱。
表1:使用AlbuPure®从CCS中捕获纯化IL-1ra和anti-HIV gp41白蛋白融合蛋白并去除宿主细胞蛋白(HCP)的色谱条件。
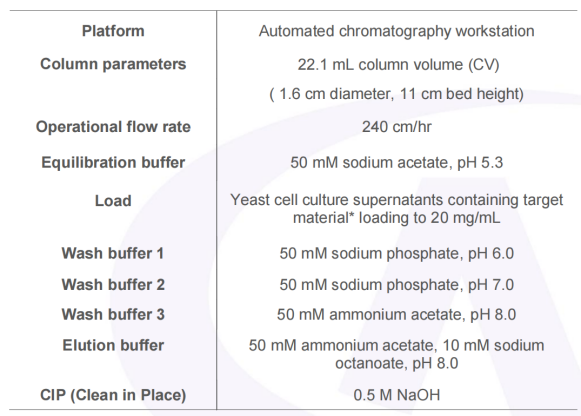
结果
结果与讨论
01
IL-1ra白蛋白融合蛋白
IL-1ra 白蛋白融合蛋白 (~85 kDa) 被 AlbuPure® 吸附剂捕获,非靶标蛋白在色谱柱中流穿。使用一系列pH值增加的缓冲液洗涤去除宿主细胞蛋白,之后使用含有辛酸钠的缓冲液选择性地从柱中洗脱白蛋白融合蛋白(图1)。通过SDS-PAGE分析工艺馏分(图2)。
图1:利用AlbuPure®从CCS中捕获和纯化IL-1ra白蛋白融合蛋白、去除HCP的色谱图。
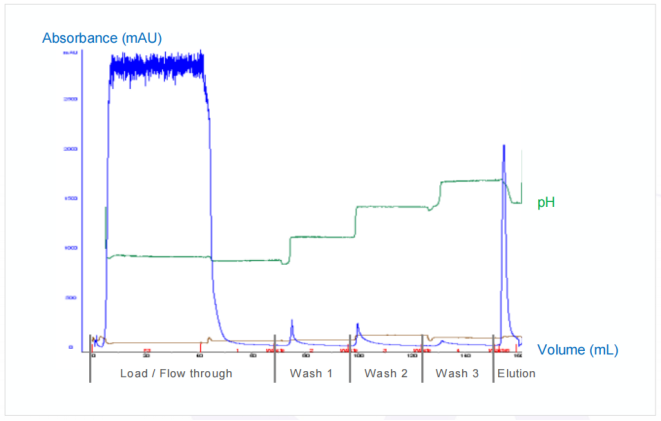
图 2: 使用 AlbuPure® 纯化的 CCS 中 IL-1ra 白蛋白融合蛋白层析组分的SDS-PAGE. Lane 1: Load (diluted); Lane 2: FT (neat); Lane 3: post load wash (neat); Lane 4: wash 1 (neat); Lane 5: wash 2 (neat); Lane 6: wash 3 (neat); Lane 7: elution (diluted); Lane 8: elution (10 fold dilution of lane 7); Lane 9: human albumin standard (1 µg).
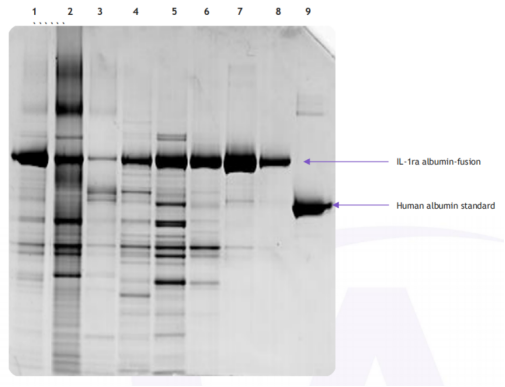
SDS-PAGE 分析(图 2)表明目标蛋白较高的结合能力,非目标蛋白在流穿液和洗涤液中(lanes 2 and 3)。增加 pH 值的洗涤步骤(lanes 4 to 6)突出表明非目标蛋白大量被清除(只有少量目标蛋白流失)。洗脱部分显示出较高的IL-1ra 白蛋白融合蛋白的纯度和回收率(lanes 7 and 8)。
参考资料:
Data courtesy of Albumedix Ltd: Use of a Novel Affinity Matrix as a Platform Purification for Albumin Fusions, Recovery of Biological Products XIV Conference presentation, Lake Tahoe, California, August 1st – 6th 2010.
来源于优宁维药物研发官网

