1957年, 自弗朗西斯·克里克提出中心法则以来,对于基因组、转录组以及蛋白质组的相关研究就从未停止过。在单细胞层面,从基因组,到转录组,再到现在的蛋白组学,表观组学,甚至于扩展到空间多组学。随着越来越多的方法被提出,研究人员对于细胞的状态及演化研究的更加细致,生物学中越来越多的机制被发现。联合多种组学,不仅可以了解单个细胞的转录机制,也可以更准确的了解其前因后果以及其调控机制,甚至发现一些更多的现象。
单细胞多组学如何分析,解决什么样的问题? 接下来,我们分享几篇文章,来看科研人员们是如何玩转单细胞多组学的。
01
单细胞转录组+空间代谢组学
2022年11月于《Cell Stem Cell》发表的《Spatial dynamic metabolomics identifies metabolic cell fate trajectories in human kidney differentiation》,该文章使用单细胞RNA测序、单细胞水平的空间代谢组学与免疫荧光结合的方式,解析了人类肾脏分化中的代谢细胞命运轨迹。首先作者基于单细胞转录组对对妊娠13周、16周、18周的人胚胎肾脏样本进行测序,这些样本覆盖了肾形成的多个阶段,例如NPCs、前管状聚集体(PTA)、肾囊泡肾小泡(RV)、逗号形小体(CSB)等。作者一共鉴定出22中细胞类型,并且发现所有22种不同的肾细胞类型都具有独特的代谢基因模式。接下来作者基于代谢基因集及拟时序分析,NPCs向每个成熟肾单位成分的分化具有特定的代谢轨迹,也可以识别出分化过程中的中间细胞类型。同时,基于拟时间评分与通路活性评分之间的前20个代谢通路分析表明,远端、近端和足细胞上皮细胞发育伴随着不同的代谢途径的变化,包括中枢能量代谢和脂质重塑。

图一:以单细胞转录组学为特征的人肾细胞代谢异质性
并且,作者基于单细胞转录组与单细胞空间代谢组联合分析揭示了人诱导多能干细胞(hiPSC)来源的肾类器官近端上皮的代谢不成熟。从单细胞转录组层面来看,共鉴定出23种细胞类型,包括主要的肾细胞类型PTs、DTs和足细胞。同时肾类器官PTs与人胎儿肾PTs具有相似的基因转录模式。基于发育中的肾细胞分类器(DevKidCC)观察到早期PT和成熟PT细胞群的存在。这些数据表明,在hiPSC来源的肾脏类器官和人胎儿肾中具有类似的PT细胞群。
应用MALDI-MSI测量从两个hiPSC系(LUMC0072和iPSC-MAFB)分化出来的hiPSC衍生的肾脏类器官发现,来自两种细胞系的肾类器官相同的细胞类型具有相似的脂质模式。然而,类器官的整体脂质组表达模式,特别是小管结构,与人类胎儿肾组织很不相同。这些都可能反映了肾类器官小管上皮的不成熟状态:尽管肾脏类器官与人类胎儿肾小管结构具有一些特征脂质物种,如m/z890.64磺基半乳糖神经酰胺等,但是在肾脏类器官中缺乏一些人胎儿肾脏中高度丰富的其他PT特异性脂质特征。
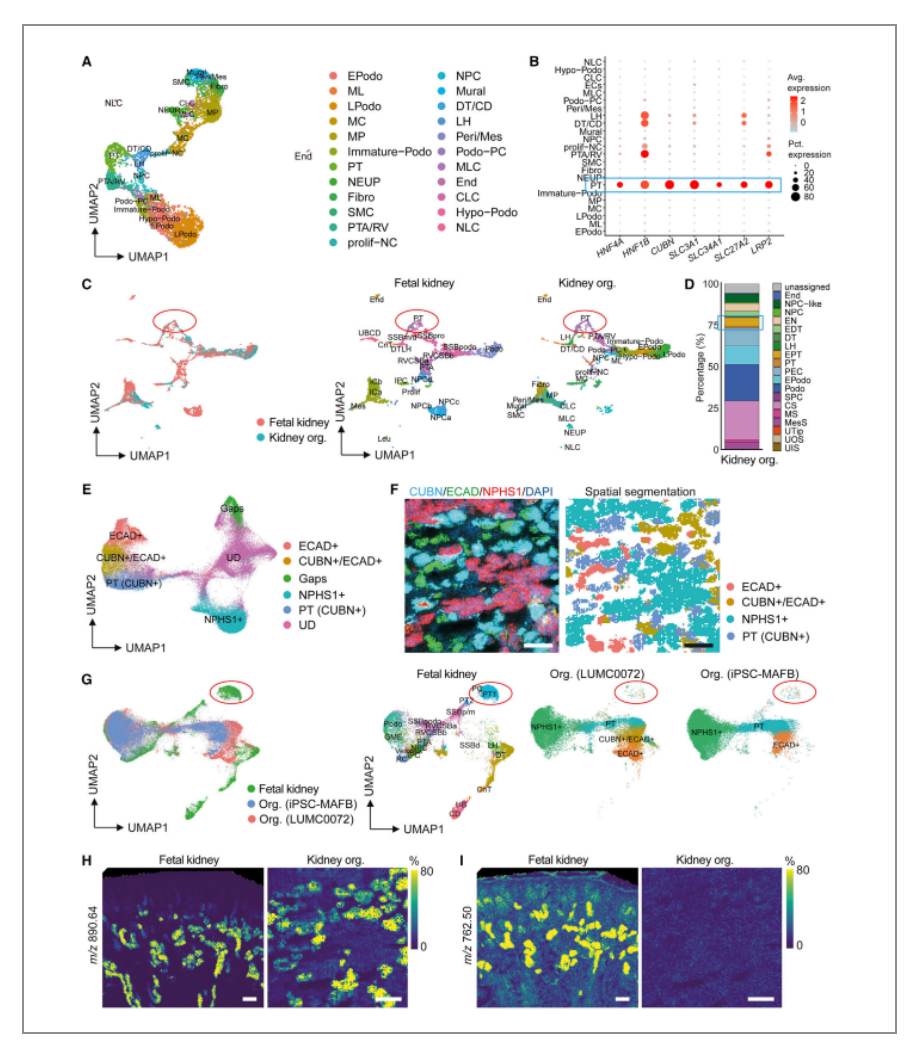
图二:hiPSC来源的肾类器官近端上皮细胞的脂质异质性和不成熟特征
02
单细胞ATAC+单细胞转录组
2021年5月发表于《Cell》的《A cis-regulatory atlas in maize at single-cell resolution》的以单细胞ATAC技术主要解释了在玉米中的顺式调控图谱,一共从玉米6种不同器官(侧芽、雄花花序、雌花花序、全苗、胚根尖以及胚后根冠)中获得56,575个单细胞核,平均31,660个独特的Tn5作用位点。通过对矩阵降维分析,一共获得了10个大群,并且这些大群可以进一步划分为92个亚群,这些不同染色质谱的亚群代表了不同的潜在细胞类型,作者也基于不同的marker基因的可及性状态来验证了部分细胞类型,例如维管束鞘特异表达的基因DCT2,SSU2以及叶肉特异表达的MDH6和PDK1。
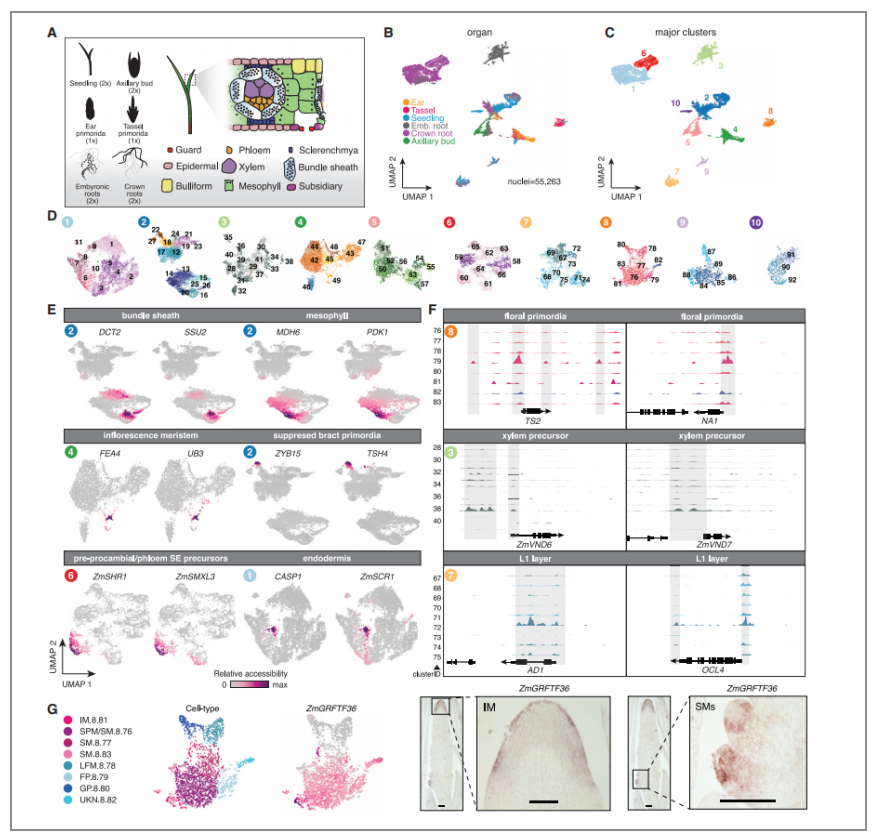
图三:玉米单细胞开放染色质可及性景观
TSS的染色质可及性是转录的前提,为了评估核转录与染色质可及性之间的关系,作者通过单细胞核RNA-seq(snRNA-seq)对15515个幼苗单细胞核进行测序,并与对应的scATACseq幼苗数据进行整合。两种组学联合分析发现19个具有相似表达谱的簇。基因变异性的比较表明了各亚群间染色质可及性和核转录的具有一致的模式,从类群间的marker基因具有非常相似的表达模式可以证明。并且通过于转录组对比,染色质可及性的亚型间差异更大,表明染色质可及性在解析细胞类型的异质性上提供了更多的信息。
同时作者发现虽然染色质可及性于上下游基因的表达存在关联,但是依然存在一部分于可及的基因并没有转录表达。这些染色质可及的不表达基因内和侧翼富集更多的H3K27me3修饰,去除H3K27me3修饰的基因提高了染色质可及性和核转录。
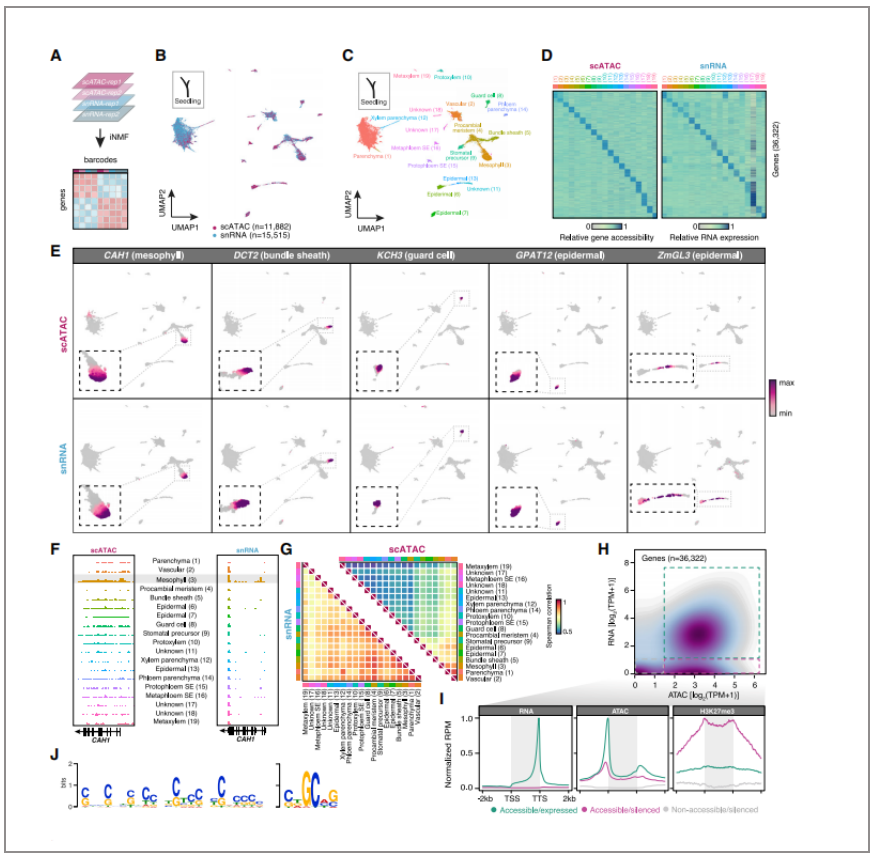
图二:单细胞ATAC与单细胞转录组联合分析
03
单细胞转录组+单细胞ATAC+Bulk RNA-seq + GWAS
2021年8月于《Nature genetics》发表了文章《Mapping the genetic architecture of human traits to cell types in the kidney identifies mechanisms of disease and potential treatments》,该文章将细胞类型通过反卷积的方法映射到Bulk RNA-seq水平上,基于659个显微解剖的人类肾脏样本队列生成了表达量性状位点(eQTLs)的综合图谱,并且通过分析细胞类型丰度和基因型之间的相互作用来解析出细胞类型依赖的eQTLs。通过使用分层连锁不平衡得分回归划分遗传性,将GWAS与单细胞RNA测序进行整合以及利用单细胞开发染色质分析,最终利用贝叶斯共定位发现了超过200个关于肾功能和高血压的基因。作者分析阐明了最常用的抗高血压和肾脏保护药物作用的关键基因基础,并确定了肾脏疾病的药物再利用机会。
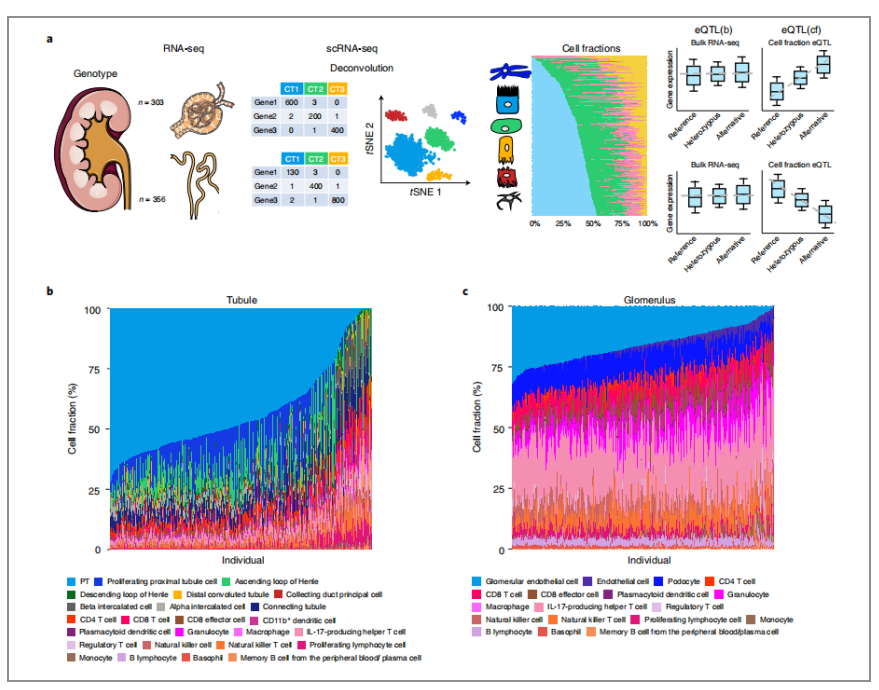
图一:利用反卷积来分解Bulk RNA-seq中的细胞类型比例

图二:基于GWAS、eQTL、scATAC等
多种组学分析方法展示了CKD和高血压的治疗靶
来源于优宁维药物研发官网

