磷酸二酯酶(phosphodiesterase, PDEs) 是一类水解cAMP 及 cGMP 的水解酶,通过选择性地水解调控蛋白和转录因子的第二信使cAMP和cGMP,在细胞内信号传导中发挥关键作用。自从E.W.萨瑟兰于1965年基于环磷酸腺苷(cAMP)在细胞的重要作用提出第二信使概念,“第二信使”就成为了一个药物发现的极其重要的工具[2]。第二信使主要有:环磷酸腺苷(cAMP),环磷酸鸟苷(cGMP),肌醇三磷酸(IP3),甘油二酯(DAG),钙离子(Ca2+)。第二信使通过其浓度变化(增加或者减少)应答胞外信号与细胞表面受体的结合,调节胞内酶的活性和非酶蛋白的活性,从而在细胞信号转导途径中行使携带和放大信号的功能。而磷酸二酯酶(PDEs)具有水解细胞内cAMP 及 cGMP的功能,降解细胞内cAMP或cGMP为5-单磷酸核苷(5’ AMP或5’GMP),从而终结这些第二信使所传导的生化作用。cAMP-PDEs和cGMP-PDEs很早就被认为是药物开发的靶点。
人PDE源于21个基因,分为11个家族(PDE1-PDE11),PDE不同起始位点的转录及其mRNA的差异剪接导致多种亚型。每种亚型在组织、细胞类型上分布不同,为开发特异性抑制剂提供了更多的机会。PDE根据其对环核苷酸的水解特异性分为三类:特异性水解cAMP (PDE4、PDE7和PDE8)、特异性水解cGMP(PDE5、PDE6和PDE9),以及能够同时水解cAMP和cGMP(PDE1、PDE2、PDE3、PDE10和PDE11)。
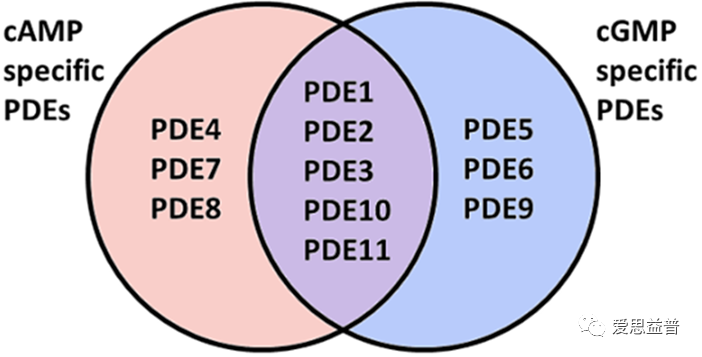
图1 :11个PDE家族的分类[7]
PDE同工酶通常以二聚体形式存在。它们的单体结构具有三个不同结构域的共同特征。N端调控域是每个同工酶家族及其变体的特征。催化结构域非常保守,与其他哺乳动物PDE催化结构域同源性为25%-52%,并含有一个Zn2+结合位点。C端结构域可以被戊酰化或被MAPK磷酸化。随着GAF结构域(cGMP激活的PDE,腺苷酸环化酶和Fh1A结合结构域)、cAMP激活的交换蛋白(EPAC)、cAMP调节的鸟嘌呤核苷酸交换因子(cAMP- GEFS)和环核苷酸门控通道(CHGC)的发现, cAMP作用的新机制得到了强调,这导致了环核苷酸相关途径的扩展和多样化。
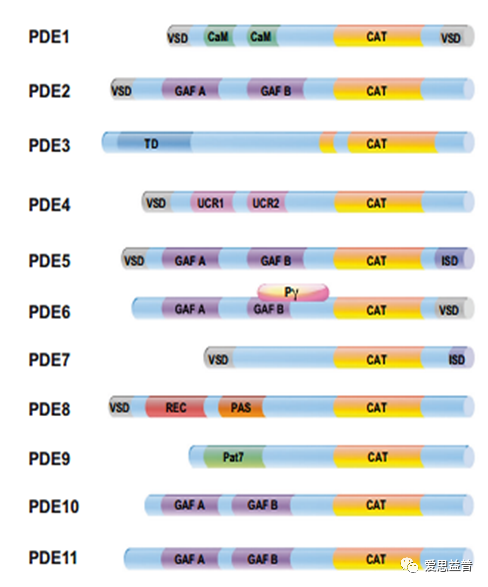
图2 :11个人类PDE家族的结构示意图[1]
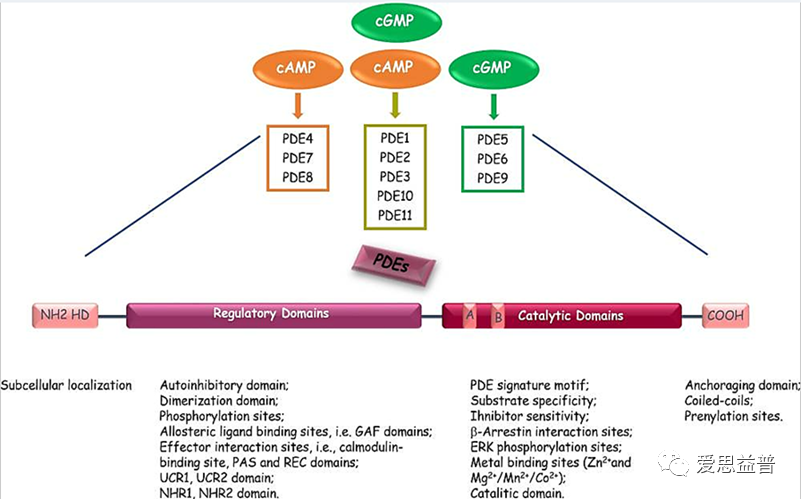
图3:不同PDE酶的共同结构[5]
通过环核苷酸途径的信号传导是许多生物系统功能的核心。cAMP通常是由激素刺激7个跨膜G蛋白偶联受体(GPCR)产生的。配体与合适的GPCR结合激活G蛋白复合物的Gsα-亚基,将GDP交换为GTP,随后从复合物中释放出来。活化的Gsα-亚基刺激膜相关腺苷酸环化酶将ATP转化为cAMP,进而激活蛋白激酶A (PKA)、EPAC或环核苷酸门控通道(CNGCs)。cGMP是通过一氧化氮(NO)或利钠肽(CNP)刺激鸟苷酸环化酶产生的。cGMP激活蛋白激酶G(PKG),PKG进而介导凋亡、炎症和其他生理过程中相关蛋白的磷酸化。PDE通过水解cAMP和cGMP的水解,进而调节它们细胞内的浓度,从而调节无数的生物效应[4]。

图4:环核苷酸信号通路[3]
PDE因其广泛的抑制效果在中枢神经系统、免疫、血液和泌尿系统疾病的发生发展发挥重要作用,成为近几年研究的热点。PDE抑制剂是用于管理和治疗慢性阻塞性肺病(COPD)、勃起功能障碍(ED)、肺动脉高压(PAH)、良性前列腺增生(BPH)、急性失代偿性心力衰竭、银屑病、银屑病关节炎(PA)、特应性皮炎(AD)和新生儿呼吸暂停的药物。在预防cAMP或cGMP降解的药物类别中,它表现出平滑肌松弛、血管扩张和支气管扩张作用。截至目前,全球已经有超过40种PDE抑制剂作为治疗药物使用,近几年研究发现PDE在多种肿瘤中异常表达,对不同PDE家族各基因亚型调控肿瘤发生发展的机制进行研究,可为肿瘤治疗提供新靶点,将成为未来PDE研究的一大重要方向。
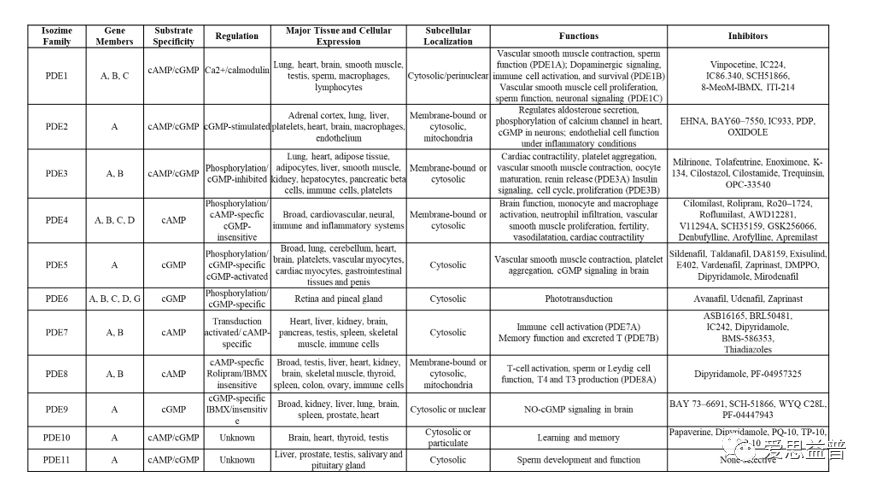
图5:PDEs家族及其抑制剂[5]
爱思益普PDE panel 筛选平台介绍
IBC打造了从蛋白纯化、靶点筛选和PDE Panel的综合性平台。其中PDE Panel筛选平台拥有PDE全部11个亚型的25个靶点的assay,旨在助力PDE靶标的抑制剂评估及选择性分析。
1
蛋白纯化
目前IBC可提供包括PDE3A、PDE3B、PDE4D2、PDE5A1等多种重组蛋白,所有蛋白产品均经过严格质控和活性验证,以满足不同实验场景的需求。
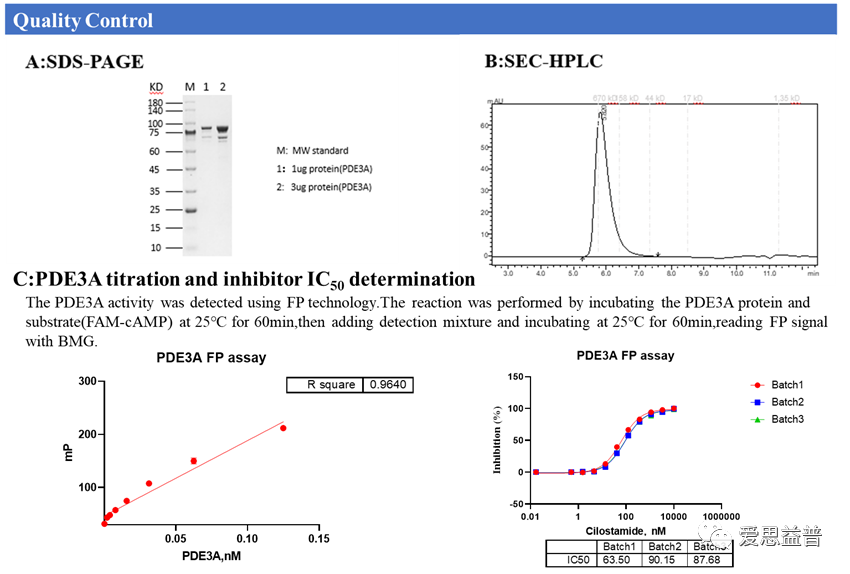
2
检测小分子对PDE蛋白作用的抑制
PDEs通过催化染料标记的环磷酸中磷酸二酯键的水解来检测其水解活性。PDE水解后暴露出核苷酸单磷酸,添加单磷酸高亲和力结合的Beads,使结合后的荧光分子复合物运动速率发生变化,从而产生高荧光偏振信号值。通过FP的方法检测PDEs对环磷酸的水解程度以反应小分子对PDEs的抑制。
针对PDE,我们使用FDA批准的上市药物或是正在开发的抑制剂作为质控分子,进行体系稳定性和灵敏性的验证,均与发表结果高度一致。
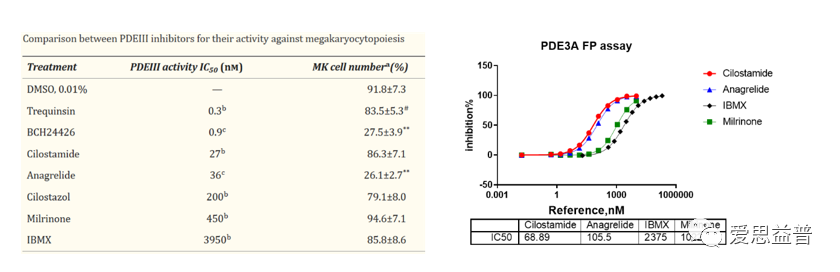
同时,我们也推出针对PDE 11个亚型,25个(包括同一亚型中不同的几个重要的同工酶)常见靶点的测试,为PDE选择性抑制剂提供全面的评价服务。对于不同亚型之间的选择性,以及针对某个亚型的选择性(例如PDE4亚型的10个靶点),我们均可提供服务。

小结
IBC团队可以提供针对PDE家族蛋白的产品及定制服务,在进行高质量的靶标筛选的同时,推出了“PDE Panel”筛选服务,对国内外数百个分子进行了活性评估。除了生化服务平台,爱思益普还可以在细胞生物学,DMPK分析,体内动物模型的药效评价以及神经心脏安全和体外次级药理学安全性评价(Safety panel)等方面拥有丰富的服务经验。对PDE相关服务感兴趣的同仁,可以随时联系我们索取资料!
参考文献
1. Delhaye S, Bardoni B. Role of phosphodiesterases in the pathophysiology of neurodevelopmental disorders. Mol Psychiatry. 2021 Sep;26(9):4570-4582. doi: 10.1038/s41380-020-00997-9. Epub 2021 Jan 7. PMID: 33414502; PMCID: PMC8589663.
2. Azevedo MF, Faucz FR, Bimpaki E, Horvath A, Levy I, de Alexandre RB, Ahmad F, Manganiello V, Stratakis CA. Clinical and molecular genetics of the phosphodiesterases (PDEs). Endocr Rev. 2014 Apr;35(2):195-233. doi: 10.1210/er.2013-1053. Epub 2013 Dec 5. PMID: 24311737; PMCID: PMC3963262.
3. Levy I, Horvath A, Azevedo M, de Alexandre RB, Stratakis CA. Phosphodiesterase function and endocrine cells: links to human disease and roles in tumor development and treatment.Curr Opin Pharmacol. 2011 Dec;11(6):689-97. doi:10.1016/j.coph.2011.10.003. Epub 2011 Oct 31. PMID: 22047791; PMCID: PMC4727450.
4. Bolger GB. The PDE-Opathies: Diverse Phenotypes Produced by a Functionally Related Multigene Family. Trends Genet. 2021 Jul;37(7):669-681. doi: 10.1016/j.tig.2021.03.002. Epub 2021 Apr 5. PMID: 33832760.
5. Barone I, Giordano C, Bonofiglio D, Andò S, Catalano S. Phosphodiesterase type 5 and cancers: progress and challenges. Oncotarget. 2017 Oct 12;8(58):99179-99202. doi: 10.18632/oncotarget.21837. PMID: 29228762; PMCID: PMC5716802.
6. Keravis T, Lugnier C. Cyclic nucleotide phosphodiesterase (PDE) isozymes as targets of the intracellular signalling network: benefits of PDE inhibitors in various diseases and perspectives for future therapeutic developments. Br J Pharmacol. 2012 Mar;165(5):1288-305. doi: 10.1111/j.1476-5381.2011.01729.x. PMID: 22014080; PMCID: PMC3372715.
7. Ercu M, Klussmann E. Roles of A-Kinase Anchoring Proteins and Phosphodiesterases in the Cardiovascular System. J Cardiovasc Dev Dis. 2018 Feb 20;5(1):14. doi: 10.3390/jcdd5010014. PMID: 29461511; PMCID: PMC5872362.
来源于优宁维药物研发官网

