在过去的十年中,体外三维模型作为先进的生物模型被开发出来,这使得人们可以深入了解细胞与细胞以及细胞与环境之间的相互作用。随着对癌症免疫治疗的关注,越来越多的工作开始使用三维模型来重建癌症中的局部或全身免疫环境。最近的进展表明了体外三维肿瘤免疫学模型具有潜在的实用性,包括在基础研究中更好地定义CIC,评估和探索免疫疗法,以及开发人工龛位辅助的“药物递送系统”(Drug Delivery System, DDS)。从而为在三维体外系统中解决实体瘤免疫治疗耐药或无效的问题提供了前所未有的机会,为进一步的理解细胞和分子机制、提高免疫治疗效果提供了多维的资源。
2023年7月4日,清华大学机械工程系生物制造团队孙伟教授/庞媛副研究员在Nature Reviews Immunology上在线发表了题为“Harnessing 3D in vitro systems to model immune responses to solid tumours: a step towards improving and creating personalized immunotherapies”的综述文章,清华大学机械工程系博士研究生周珍珍为该文章的第一作者,清华大学机械工程系生物制造团队庞媛副研究员和孙伟教授为本文的共同通讯作者。作者针对实体瘤现有免疫疗法的局限性,全面回顾了各种体外三维建模技术,并强调这些技术如何应用于模拟和再现CIC,以评估免疫治疗策略进而探索免疫治疗的优化方案及个性化的肿瘤免疫治疗。最后,针对该研究领域的挑战和重要发展机遇进行了评述和展望。
免疫疗法可以局部改变肿瘤微环境(Tumor Microenvironment, TME)或系统改善免疫监视,这些疗法明显推动了血液肿瘤的治疗。然而,大多数实体瘤患者无法从目前的免疫疗法中获益。CIC的巨大复杂性、异质性和适应性导致了对免疫疗法的不同反应。
免疫治疗抵抗或无效的机制可分为以下几类:首先,局部TME和全身免疫反应的免疫抑制环境可能导致驻留或浸润的细胞毒性免疫细胞失活或衰竭,如“细胞毒性T淋巴细胞”。其次,局部TME的变形结构和血管高渗渗漏对治疗性细胞浸润或药剂输送构成了物理屏障。三,由于TME和系统免疫反应的异质性,治疗性基因改造细胞上的特定分子结构总是导致反应的可变性和免疫抵抗。例如,实体瘤含有携带逃逸变体的细胞,可以逃避“嵌合抗原受体T细胞”(Chimeric Antigen Receptor T cell, CAR T cell)的定位。第四,有限的或不适当的给药方案导致疗效下降和副作用增加。然而,解决所有这些挑战是传统的肿瘤模型系统,即二维共培养和动物模型所不能及的。
1. 基于支架的三维模型
在基于支架的三维模型中,细胞被植入到模拟实体组织的细胞外基质(Extracellular Matrix, ECM)的生物材料中(图1)。三维支架可通过自由堆叠不同形态的微颗粒或集成结构来建立。细胞接种是在微孔或纤维支架上进行的,支架的制备采用了不同的配制工艺(如两相乳化、发泡、冷冻干燥和静电纺丝)。支架平台可对递送的免疫调节剂和免疫细胞之间的相互作用进行时空调节,并重现免疫细胞的串扰。通过调整支架材料,研究ECM的物理和生物化学特性如何影响免疫治疗反应和免疫细胞功能。
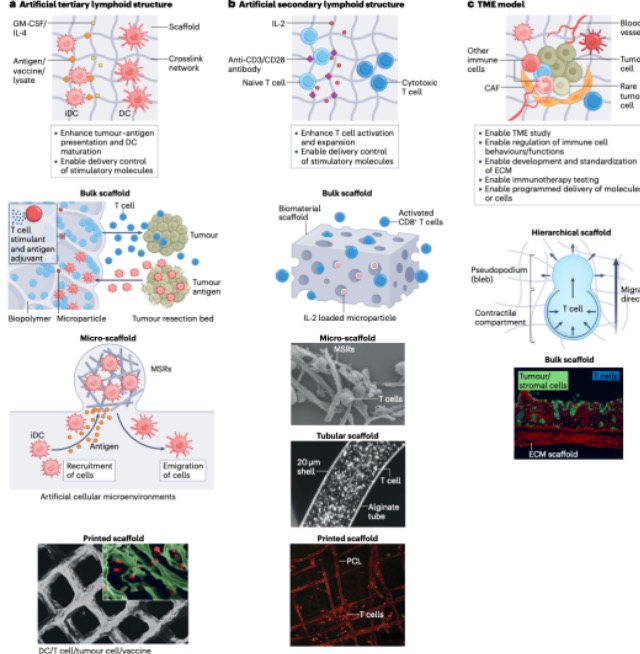
图1. 用于肿瘤免疫学研究的基于支架的三维模型示意图
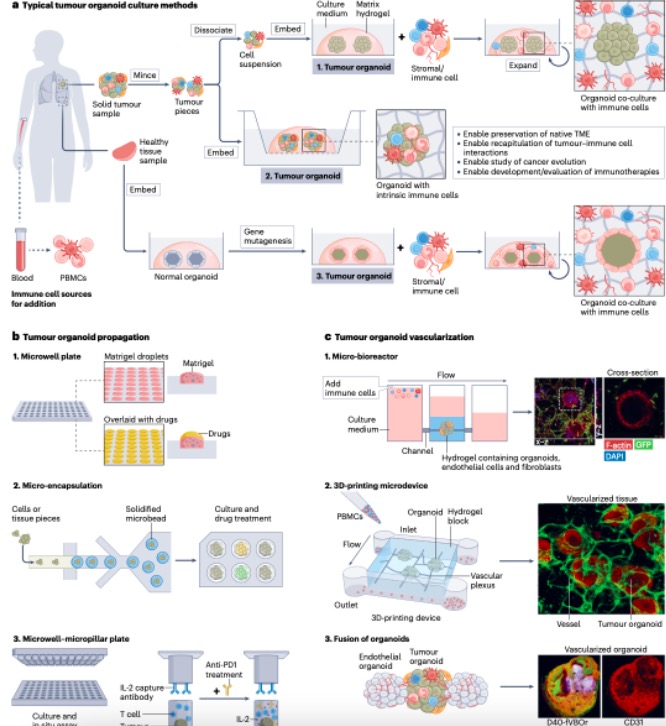
图2. 用于肿瘤免疫学研究的肿瘤类器官模型示意图
3. 微流体3D模型
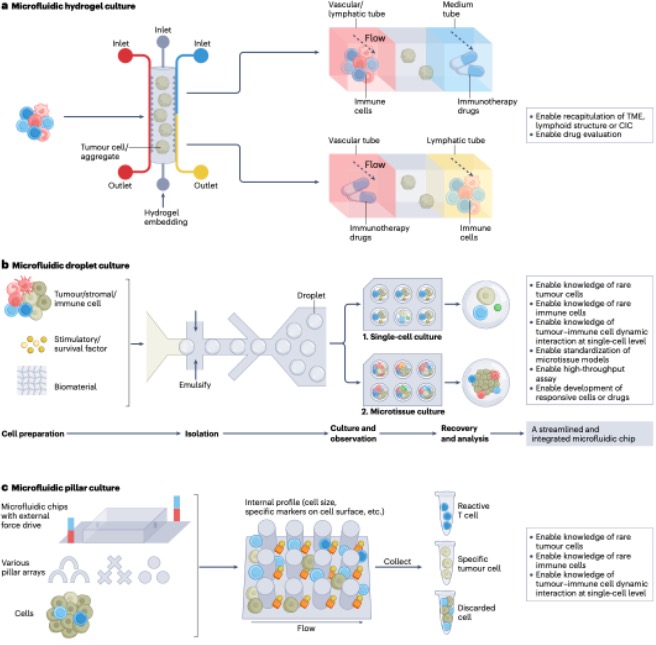
图3. 用于肿瘤免疫学研究的微流控三维模型示意图
4. 基于生物打印的三维模型
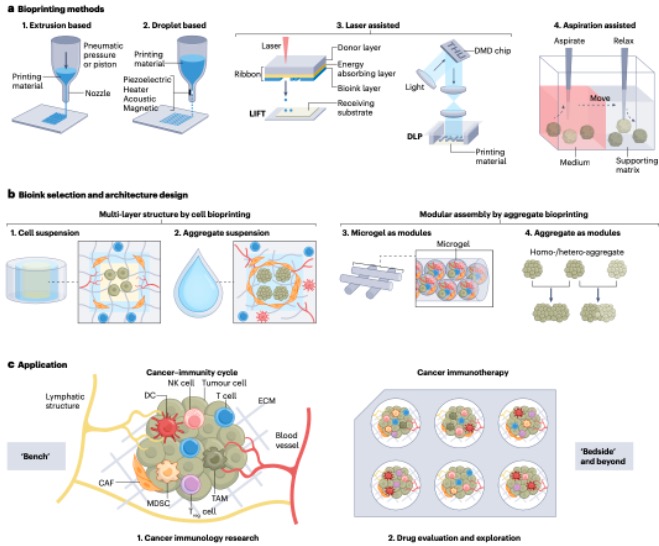
图4. 用于肿瘤免疫学研究的基于生物打印的三维模型示意图

