近几年,细胞和基因治疗(cell & gene therapy,CGT)领域发展迅猛,在多个方向取得了重大突破,以anti-CD19和BCMA为代表的多种CAR-T免疫细胞疗法攻克了一部分血液瘤,多种AAV疗法也给一些难以成药的罕见病提供了有效的治疗方案。另一方面,基于CRISPR基因编辑技术的众多基因疗法也进展迅速,首个体外基因编辑疗法最快今年年底能够上市(CRISPR Therapeutics CTX001)[1],体内基因编辑疗法取得了不错的临床数据(Intellia Therapeutics NTLA-2001)[2],使用CRISPR技术制造的通用型CAR-T疗法也是免疫细胞疗法发展的一大趋势(Caribou Biosciences CB-010)[3]。
CRISPR基因编辑治疗发展如火如荼,但也有不少人对基因治疗的安全性提出担忧,由于CRISPR技术是直接改变基因组DNA,其中任何的改变都会被永久保留下来,所以CRISPR对于DNA序列的任何改变都需要严谨的安全评估。根据目前已经公开的FDA关于基因治疗的指导文件[4],对于基因治疗安全性的评估可以简单总结为两个方面:
-
Assessment of genomic integrity, including chromosomal rearrangements, large insertions or deletions, integration of exogenous DNA, and potential oncogenicity or insertional mutagenesis. -
Identification of off-target editing activity, including the type, frequency, and location of all off-target editing events.
脱靶位点检测技术盘点
-
细胞外检测方法
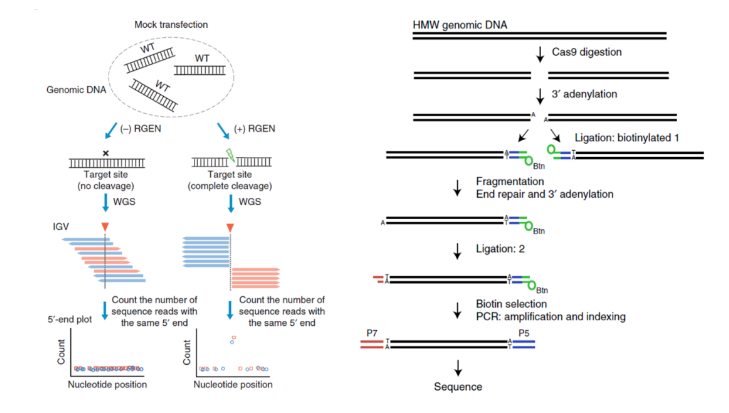
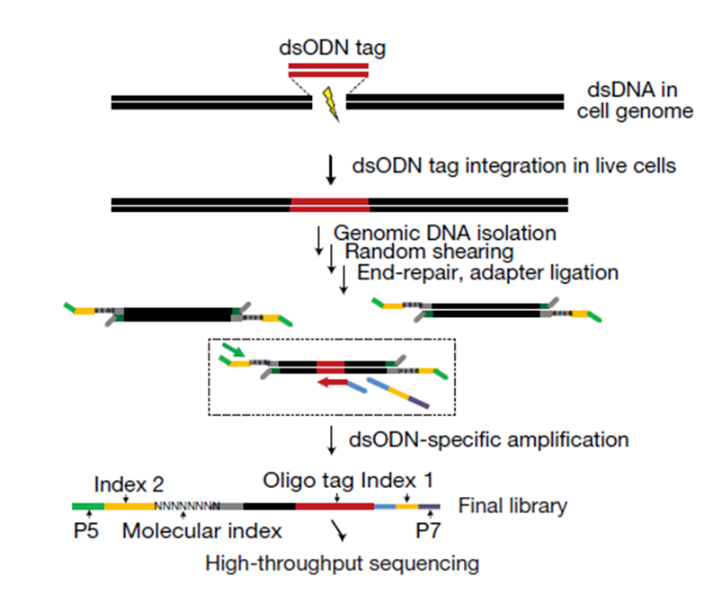
总结
不论在科研还是临床中,CRISPR技术的使用都带来了非常高的回报,也同时伴随着各种风险,这其中脱靶现象就研究者们最为担心的一类风险。本文中我们盘点了多种主流的CRISPR脱靶位点检测方法,但没有一种方法是适用于所有CRISPR技术的脱靶检测,一个项目中只使用一种脱靶检测方法也是不足够的。如何在实验中,特别是临床试验中全面评估CRISPR的脱靶风险,需要将多种脱靶检测方法有效组合。同时,每一条sgRNA都不可避免地存在脱靶位点,如何评估这种风险,如何降低这种风险,具体的解决方案我们会在下一期的文章中,用临床实例来为大家介绍。

