单克隆抗体在抗击新冠病毒中发挥着关键作用,并已被证明能有效减少患者症状由轻症向重症的发展。然而,该领域未来的进展取决于抗体开发的时间和技术。近日,《Nature - Scientific Report》杂志发表的一篇文章论证了单B细胞克隆筛选在快速、可靠地识别高亲和力、强效的新冠病毒(SARS-CoV-2)中和抗体方面的应用,并解释了如何增强其中和活性。
中和抗体
疫苗接种后,一般会产生不同类型的抗体,以中和抗体为例:中和抗体由病毒最外层的包膜或衣壳抗原刺激机体产生的一类能与病毒结合并使之丧失感染力的抗体。目前针对新冠疫苗的研究中,中和抗体属于研究的热点,如针对S1蛋白的受体结合域(receptor-binding domain,RBD)、针对S1蛋白的N末端域(NTD)。
该研究中研究的中和抗体属于前者,针对S1蛋白受体结合域(RBD),它可以和SARS-CoV-2的RBD区域结合,阻断该区域与血管紧张素转化酶II受体(ACE2 receptor)的结合,从而达到阻止病毒入侵细胞的功效。该类抗体是人体产生的最多、最主要也是阻断病毒效果最好的一类抗体。
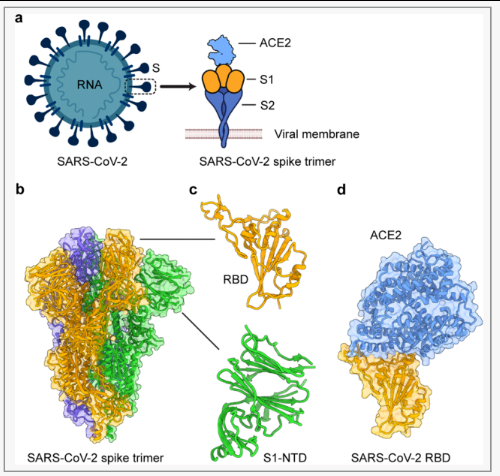
图1. SARS-CoV-2刺突(S)的蛋白结构。a. SARS-CoV-2病毒粒子及其S蛋白示意图。E包膜,M膜,N核衣壳,血管紧张素转换酶2。b. SARS-CoV-2 S蛋白三聚体(PDB 6VXX)低温em结构。分别用橙色、绿色和蓝色三种颜色来表示这三个亚基。c. SARS-CoV-2 S受体结合域(RBD)和S1亚基n端结构域(NTD)。d. SARS-CoV-2 RBD与人ACE2复合物的晶体结构(PDB 6M0J)。人类ACE2是浅蓝色的
通过单B细胞筛选,可以更快发现抗体
通过单B细胞分选,可以将抗体的发现过程缩短至几周之内。这种开创性的方法包括从免疫动物或康复患者中分离活细胞,分类抗原特异性细胞亚群,并通过RT-PCR和PCR恢复成对的VH/VL抗体基因; 编码的抗体可以被表达和表征,以确定性能最好的克隆,如图2所示:
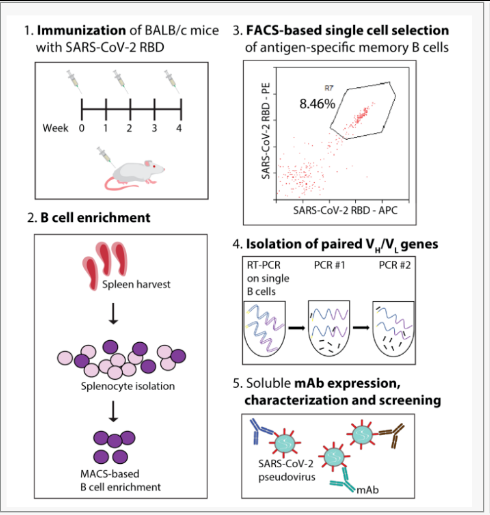
图2. 从单个B细胞中分离发现有效的SARS-CoV-2中和抗体并进行鉴定的方法综述
该方法的优点是使用了经过体细胞高突变的原生抗体序列,并保留了原生VH/VL配对。此外,发现过程是高通量的,可以进一步对高免疫抗体库进行评估。
针对SARS-CoV-2病毒的中和抗体
为了评估单B细胞筛选在分离针对SARS-CoV-2病毒的中和抗体的有效性,研究人员在HEK293T细胞中制备了一种重组形式的SARS-CoV-2受体结合域(receptor-binding domain,RBD),并对其进行蛋白纯化。
接着对BALB/c小鼠进行免疫后,通过单细胞分选从脾脏材料中分离anti‑RBD IgG1+B细胞,并处理VH /VL基因。将得到的VH/VL基因对克隆到哺乳动物表达质粒(含人IgG1恒定区和用于嵌合抗体表达的kappa轻链区)中,瞬时转染到HEK 293-6E细胞中。抗体鉴定包括Protein A磁珠的纯化、抗原结合能力、中和活性等性能的评估。
亲和性分析
在重组抗体被生产出来后,必需对其的亲和力进行分析,以便进行下游的相关应用。抗体亲和力的检测方法包括生物膜干涉技术(BLI)、固相放射免疫法(SP-RIA)、平衡透析法、结合抗原沉淀法、放射免疫法(RIA)、ELISA法、表面等离子共振法(SPR)。
该方法使用了结合抗原沉淀法进行亲和力的分析,将链霉亲和素-磁珠与包被有生物素化RBD一起孵育后,洗涤去除掉未结合的抗体。接着使用Alexa Fluor®647荧光二抗(山羊来源,抗人IgG,Fc片段特异性亲和纯化二抗,Jackson ImmunoResearch)进行孵育并通过流式细胞术进行分析。结果显示,两个克隆体(12H2和13I1)对RBD具有较低的pM EC50值,其值与先前报道的一种有效中和抗体CB6相当(图3)。
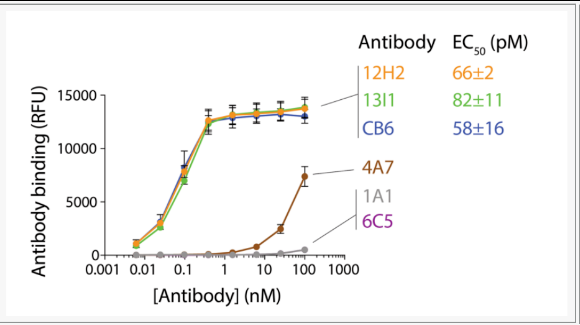
图3. 分离出的抗体与SARS-CoV-2受体结合区域具有高度亲和力。
特异性分析
将带有His标签的SARS-CoV或SARS-CoV-2的RBD区域分别与Dynabeads™磁珠进行孵育,以检测中和抗体的特异性。将这两种磁珠与不同浓度的抗体分别进行孵育,并将未结合的磁珠洗脱。接着使用Alexa Fluor®488荧光二抗(山羊来源,抗人IgG,Fc片段特异性亲和纯化二抗,Jackson ImmunoResearch)进行孵育并通过流式细胞术进行分析。
同时,研究人员评估了包被13I1抗体的磁珠与野生型SARS-CoV-2 S1蛋白以及两种变体(B.1.1.7和B.1.351)的S1蛋白结合情况。具体实验方法是将珠子与SARS-CoV-2 S1蛋白孵育,然后添加鸡属来源的抗his标签抗体,并使用Alexa Fluor®647 荧光二抗(驴来源,抗鸡IgY,F(ab’)₂片段亲和纯化二抗,Jackson ImmunoResearch),接着进行流式细胞检测。
数据显示,13I1与B.1.1.7的结合保留了下来,但与B.1.351的结合基本消失,说明B.1.351这种变体的蛋白可能通过某种机制逃脱了SARS-CoV-2抗体的结合(图4)。
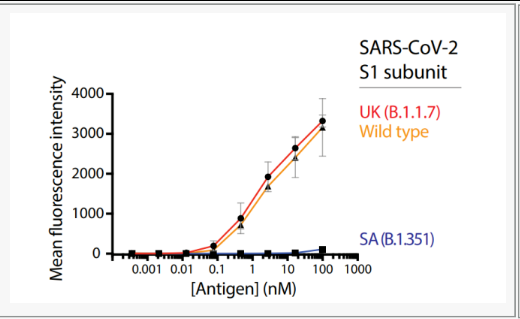
图4. 13I1抗体与SARS-CoV-2 S1亚基变异的亲和性分析
研究还显示,中和抗体具有较高的特异性和稳定性。如图5A所示,未特异性结合的抗体通过与CHO细胞中生物素化的可溶性膜蛋白孵育进行分析,并通过流式分析法来检测。两种抗体:高非特异性结合(emibetuzumab)和低非特异性结合(elotuzumab),作为对照抗体。两种对照抗体与实际药物并不完全相同,因为它们具有实际药物的可变区域和共同的IgG1框架。
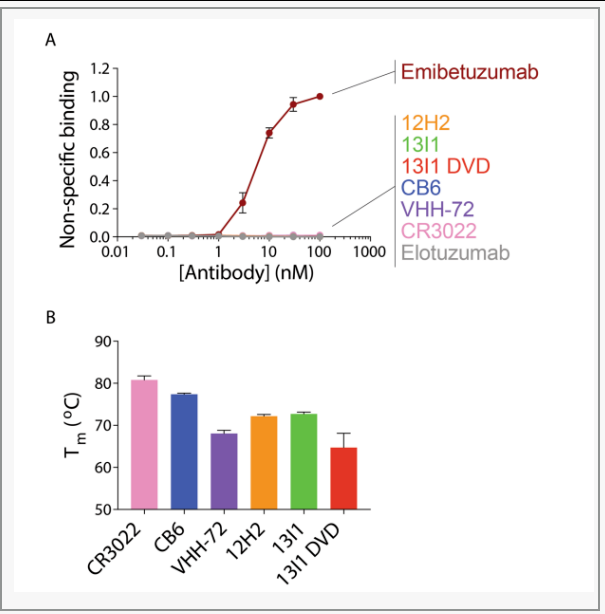
图5. 中和抗体具有较高的特异性和稳定性
中和活性
通过与显示SARS-CoV-2刺突蛋白和包含荧光素酶编码RNA的伪病毒颗粒共孵卵来评估每个抗体的中和活性。将每种混合物进行一系列稀释,然后应用于稳定表达人ACE2 (SARS-CoV-2入侵宿主细胞的细胞受体)的工程HEK293T细胞,并通过检测感染48小时后荧光素酶的相对表达量来量化假病毒的传染性。抗体12H2和13I1均具有亚nM的中和活性,IC50值分别为0.109和0.162 nM; 与CB6 (0.087 nM)的IC50相当。
通过技术手段提高中和活性
为了研究合价对中和活性的影响,文章作者设计了一个四价双可变域(DVD) 13I1抗体,并使用SARS-CoV-2假病毒试验与二价13I1 IgG进行了并排比较。DVD显示,相对于二价13I1抗体,其中和活性增强(IC50值分别为0.131 nM和0.324 nM),突显出其作为一种治疗策略的潜力。
总结
B细胞筛选已被证明可以快速识别高亲和力、强效的SARS-CoV-2中和抗体。此外,将其与抗体改良结合使用有望成为预防新冠的有效策略。
文章部分相关产品:
|
货号 |
产品名 |
|
|
Alexa Fluor® 647 AffiniPure Goat Anti-Human IgG, Fcγ fragment specific |
|
|
Alexa Fluor® 488 AffiniPure Goat Anti-Human IgG, Fcγ fragment specific |
|
|
Alexa Fluor® 647 AffiniPure F(ab’)₂ Fragment Donkey Anti-Chicken IgY (IgG) (H+L) |
|
|
CHO host cell protein ELISA kit |
|
|
Protein A/G PLUS-Agarose |
|
|
FcR Blocking Reagent, mouse |
|
|
CD45R (B220) MicroBeads, mouse |
|
|
LS Separation columns |
|
|
MidiMACS Separator |
关于Jackson Immunoresearch
Jackson ImmunoResearch Inc.是美国著名的二抗生产商。30年的专注,30年的发展,JIR公司的各种酶标(如鼠兔酶标二抗)及荧光二抗(Alexa Fluor系列,Cy3/Cy5,PE等荧光标记),种类丰富(物种齐全,标记多样,应用广泛),性价比高。
上海优宁维生物科技股份有限公司作为二抗金标准Jackson的全国代理商,携手Jackson为广大科研及工业客户带来品质优良价格实惠的各类二抗产品。
关于优宁维
上海优宁维生物科技股份有限公司(简称:优宁维,股票代码:301166)自2004年成立以来一直专注于抗体及相关产品,是国内专业、全面的抗体供应商和抗体专家,十多年来,已逐渐发展成为生命科学一站式服务商。我们长期聚焦于生命科学、生物医药、医疗诊断、分析检测等领域,提供460多万种以抗体为核心的生命科学试剂、耗材、仪器、软件、定制、实验室服务、供应链服务等,形成了以第三方品牌产品为主、自主品牌产品为辅的全面供应体系。
了解更多有关优宁维的信息,请访问:www.univ-bio.com
参考文献:
1.Schardt JS, Pornnoppadol G, Desai AA, Park KS, Zupancic JM, Makowski EK, Smith MD, Chen H, Garcia de Mattos Barbosa M, Cascalho M, Lanigan TM, Moon JJ, Tessier PM. Discovery and characterization of high-affinity, potent SARS-CoV-2 neutralizing antibodies via single B cell screening. Sci Rep. 2021 Oct 20;11(1):20738. doi: 10.1038/s41598-021-99401-x. PMID: 34671080;
2.Du L, Yang Y, Zhang X. Neutralizing antibodies for the prevention and treatment of COVID-19. Cell Mol Immunol. 2021 Oct;18(10):2293-2306. doi: 10.1038/s41423-021-00752-2. Epub 2021 Sep 8. PMID: 34497376; PMCID: PMC8424621.
推荐阅读:
+
+

